Für die weiteren Untersuchungen der thermischen Energie (Wärmeenergie) ist es zwingend notwendig, die Begriffe innere Energie und Temperatur zu unterscheiden. Für beide Begriffe ist eine Vorstellung vom Teilchenmodell grundlegend, bei der wir uns alle Stoffe zusammengesetzt aus vielen kleinen Teilchen vorstellen.
Die Temperatur ist ein Maß für die durchschnittliche Bewegungsenergie der Teilchen.
Die Temperatur ist also ein Begriff, der unabhängig von der Anzahl der Teilchen und damit auch unabhängig von der Masse des Objekts ist.
Die innere Energie eines Körper berücksichtigt jedoch auch die Anzahl der Teilchen.
Die innere Energie ist die Summe der Bewegungsenergien aller Teilchen. Damit ist die innere Energie abhängig von der Anzahl der Teilchen. Je größer die Teilchenanzahl und auch je größer die Temperatur ist, desto größer ist die innere Energie.
Beispiel zur Unterscheidung der inneren Energie und der Temperatur
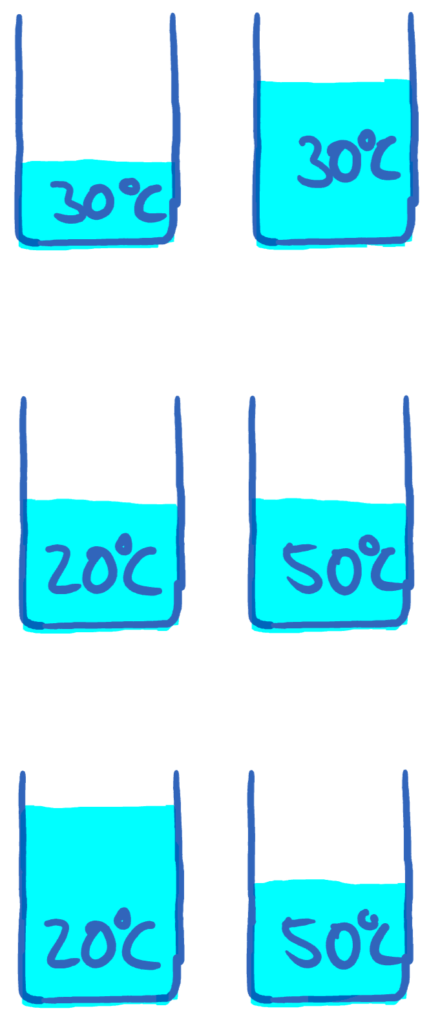
Wir betrachten die drei nebenstehenden Beispiele:
- Im ersten Beispiel ist die Temperatur in beiden Fällen gleich. Da jedoch im zweiten Behälter mehr Wasser enthalten ist, muss hier auch die innere Energie größer sein.
- Im zweiten Beispiel ist die Wassermenge in beiden Behältern gleich. Da jedoch im zweiten Behälter die Temperatur größer ist, muss hier auch die innere Energie größer sein.
- Im dritten Beispiel ist die Wassermenge im ersten Behälter größer. Dafür ist aber die Temperatur im zweiten Behälter größer. Hier ist eine Aussage über die innere Energie nicht möglich. Erst mit weiterem Wissen (und genaueren Angaben) kann eine Aussage über die innere Energie getroffen werden.
